Frontiers in oncology最新:allo-HSCT前减低强度与清髓性预处理方案有效性一致且更安全!
既往研究显示:对于完全缓解(CR)和骨髓增生异常综合征(MDS)的急性髓系白血病(AML)患者,异基因造血干细胞移植(allo-HSCT)前的减低强度预处理(RIC)与清髓性预处理(MAC)具有相同的总生存期(OS)。
然而,这个结论尚无法“盖棺定论”——不同研究的结果相互矛盾。因此,高博医学(血液病)北京研究中心北京博仁医院吴彤主任团队宋艳智医生对相关随机对照试验(RCT)进行了荟萃分析(meta-analysis)以及系统评价(SR),该研究成果于10月7日发表于Frontiers in oncology(影响因子=6.244)。

投石问路——RIC方案是否能达到低毒高效的双赢
异基因造血干细胞移植(allo-HSCT)为治疗急性髓系白血病(AML)或骨髓增生异常综合征(MDS)复发风险最低的治疗方式。然而,allo-HSCT中传统清髓性预处理(MAC)方案,与严重不良事件高风险和高非复发死亡率(NRM)相关。近三十年来,开发毒性较小、耐受性较强的移植前预处理方案——减低强度预处理(RIC)方案成为临床研究的重点。
具体而言,RIC方案预处理时,指全身放疗(TBI)总剂量小于8Gy,或白消安(Bu)总剂量小于8mg/kg(口服或等效静脉剂量),或不采用TBI或者Bu作为清髓方案,应用其他具有高效能免疫抑制作用但组织毒性较小的药物替代TBI或Bu。同时,可以用氟达拉滨(Flu)替代毒性较大的环磷酰胺(Cy)。
RIC可减少组织损伤,从而降低急性移植物抗宿主病(aGVHD)和其他并发症的发生率,一些非随机对照研究报道,RIC可降低NRM但增加疾病复发,通常导致与MAC相同的总生存期(OS)。然而观察性研究并非随机分配,结论可能会受到混淆因素的影响。
RIC与MAC方案的OS有无差别尚未定论,但在真实世界临床实践中,接受RIC的患者数量正在迅速增加。以美国为例,RIC方案占所有allo-HSCT的50%以上。因此,亟需高级别的循证医学证据来解决该临床问题,宋艳智医生开展了比较RIC与MAC治疗完全缓解的AML或MDS的疗效和安全性的系统评价和Meta分析。
尘埃落定——RIC方案OS并无差异,NRM更优!
检索了1980年1月1日至2020年7月1日期间PubMed、Web of Science、Embase、Cochrane central、临床试验登记中心和相关网站、主要会议论文集和手工检索了相关期刊中比较完全缓解的AML或MDS患者首次allo-HSCT前RIC与MAC的研究,仅纳入随机对照试验(RCT)。OS为主要终点,而次要终点为无白血病生存期(LFS)、累积复发率(CIR)、NRM、aGVHD和慢性(c)GVHD。采用最长随访数据。
共检索了7770条记录,纳入的6项研究包括1413例受试者(RIC组711例,MAC组702例)。4项研究比较了RIC与基于TBI/Bu的MAC,而2项研究比较了RIC与基于苏消安的MAC方案。研究使用外周干细胞和骨髓作为干细胞来源,供体包括匹配的亲缘、不匹配的亲缘和匹配的无关供体,以上研究中试验组与对照组基线特征均均衡。
分析结果显示:RIC vs. MAC的OS(HR=0.95,95%CI 0.64-1.4,P= 0.80;图1)和CIR与MAC(HR=1.18,95%CI 0.88-1.59,P=0.28;图2)相同。
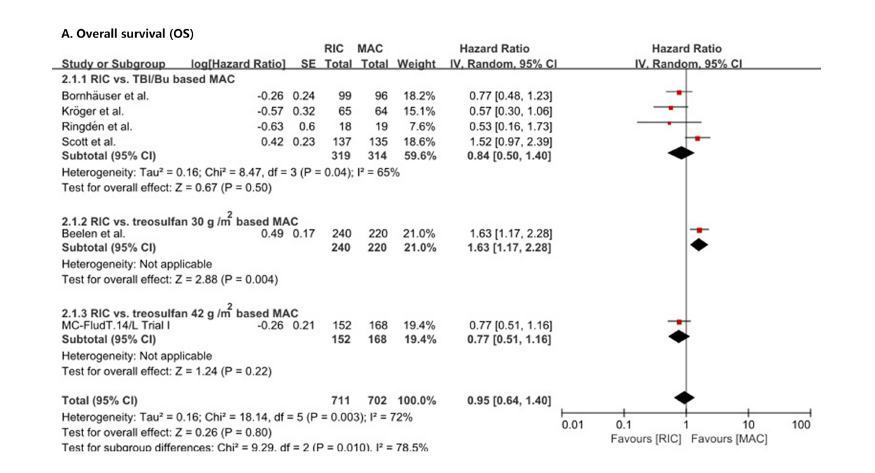
图1 meta-analysis的OS结果
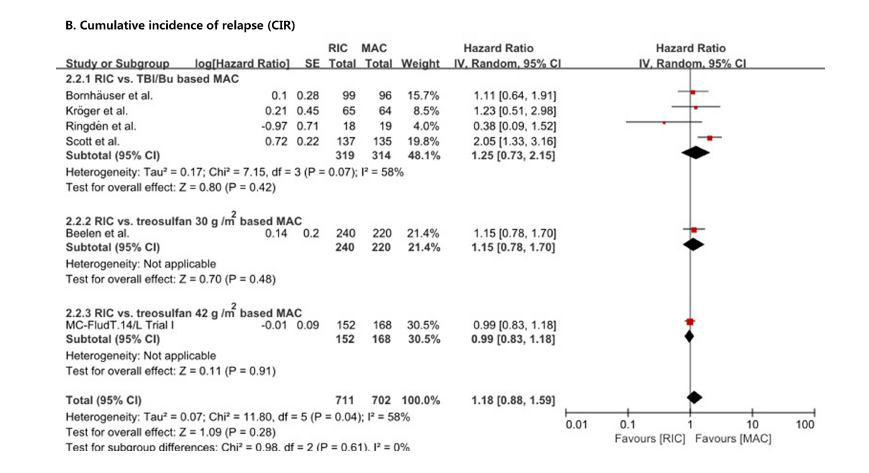
图2 meta-analysis的CIR结果
此外,与TBI/白消安为基础的MAC相比,RIC显著降低了NRM(HR=0.53,95%CI 0.36-0.80,P=0.002;图3)。
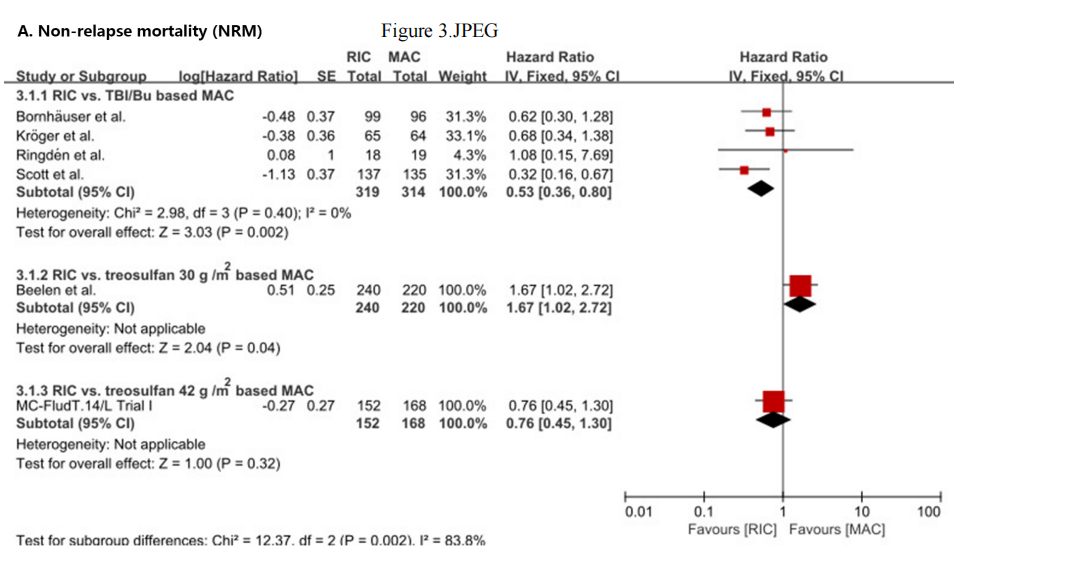
图3 meta-analysis的NRM结果
与基于TBI/Bu的MAC(HR=0.79,95%CI 0.60–1.03,P=0.08)和(RR= 0.61,95%CI 0.36–1.04,P=0.07)相比,RIC显示出减少aGVHD和III-IV aGVHD的趋势,无显著(P=0.15和P=0.19)异质性(I²=43%)和(I²= 39%)。
剑指精准——未来需进一步确认RIC方案获益人群
本研究开创性地阐明了RIC与MAC的疗效和安全性,是目前为止循证医学证据级别最高的研究。根据目前的临床研究的证据,对于完全缓解的急性髓系白血病和MDS患者,RIC不增加复发率,相对于含TBI/Bu的MAC预处理方案,降低了非复发死亡率,感染和器官功能损伤等并发症发生率也明显降低,而且,患者的耐受性更好。
虽然目前的研究结果存在异质性,仍然可以证明针对完全缓解对AML和MDS患者,RIC方案是异基因造血干细胞移植前预处理方案的良好选择。
