博医荟丨吴彤主任:造血干细胞移植相关的血栓性微血管病的诊治
本期为您分享,吴彤主任关于造血干细胞移植相关的血栓性微血管病诊治。点击上图,可查看高博医学论坛系列学术活动内容。
造血干细胞移植相关的血栓性微血管病(HSCT-associated thrombotic microangiopathy,简称TA-TMA) ,是HSCT后严重的合并症,重症TA-TMA死亡率高。TA-TMA经过治疗后的康复者常伴有高血压、慢性肾病、胃肠道和中枢神经系统症状及肺动脉高压等后遗症。
TA-TMA本质上为各种诱因导致的小血管内皮细胞损伤,血栓形成,从而引起多器官功能障碍(肾、肺、肠道、心脏、脑)。症状类似血栓性血小板减少性紫癜(TTP)及溶血尿毒综合征(HUS),但本质上是不同的疾病,TA-TMA为补体异常激活参与发病。
01
TA-TMA的发病机制
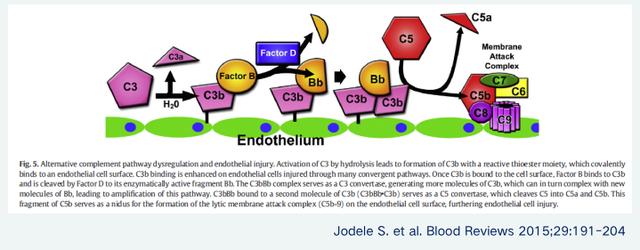
TA-TMA目前的发病机制学说为三打击学说。第一打击为个体差异,有些患者容易补体异常激活,考虑与种族、补体相关基因的变异以及遗传易感基因相关。第二打击为内皮损伤,主要与治疗相关,比如化疗、放疗会对组织造成损伤。第三打击为最后的诱因,比如常用的预防和治疗移植物抗宿主病(GVHD)的环孢素、他克莫司、西罗莫司等药物可能诱发TA-TMA。另外,GVHD、感染、针对内皮保护因子的抗体产生等因素都可能会导致TA-TMA的发生。TA-TMA的发病本质为补体异常激活导致内皮损伤,是一系列的连锁反应,先是C3的激活,最后导致了C5的激活,形成膜攻击复合物,导致内皮的损伤(图一)。
图一. TA-TMA的发病机制:补体激活与内皮损伤
02
TA-TMA的病理改变与发生部位
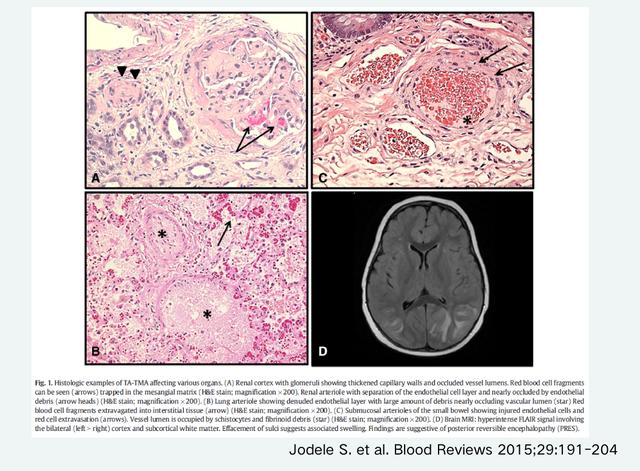
TA-TMA常累及的器官为肾脏、肠道、肺和脑,从图二可以看到TA-TMA的病理改变,内皮细胞与血管壁发生分离,均发生在与毛细血管相连的小动脉或者再上一级的小动脉,但不累及静脉和大动脉。可见红细胞碎片堵塞管腔或外渗,血管内形成血栓,小动脉管腔闭塞或者狭窄,造成组织坏死。
一项日本学者的研究通过对165例HSCT后的尸体解剖发现,有38例(23%)存在TA-TMA,其中肾脏(61%)和肠道(53%)是最常受累的器官,肾及肠道TA-TMA并存的占13%,合并GVHD在肠道TA-TMA比肾脏TA-TMA更常见(80% vs. 22%, p=0.0016),肠道GVHD是肠道TA-TMA的危险因素。
特别要关注的是小肠受累发生率为47%,大肠受累发生率仅为21%,这提示我们当临床怀疑肠道TA-TMA时,建议通过无痛肠镜进行结肠与回肠的检查并同时在上述部位取活检,以减少漏诊率。另外TA-TMA有8%发生在胃,5%发生在胆囊,少数病例发生在口腔、咽部、食道、肝脏、心脏、膀胱及输尿管。
图二. TA-TMA的病理改变
03
TA-TMA的发生率与危险因素
TA-TMA的发生率各家报道不一,约10%~39%,主要原因为有的是靠临床诊断,有的是靠病理诊断。
关于TA-TMA发生的危险因素,首先自体移植与异体移植都可能会发生,儿童和成人也都可能发病。目前的认识是,它与种族和遗传易感基因有关,另外,大剂量的化疗与放疗可能会造成TA-TMA的发生,特别是二次移植的病人比第一次移植者发生率增高。配型不合的移植会增加TA-TMA的发生,常用的预防和治疗GVHD的药物,如环孢素、他克莫司、西罗莫司可能诱发TA-TMA。此外GVHD是TA-TMA的重要诱因,很多TA-TMA的病人同时伴有GVHD,如80%的肠道TA-TMA合并GVHD。感染也是一个重要的诱因,比如:病毒感染、细菌感染、真菌感染等。
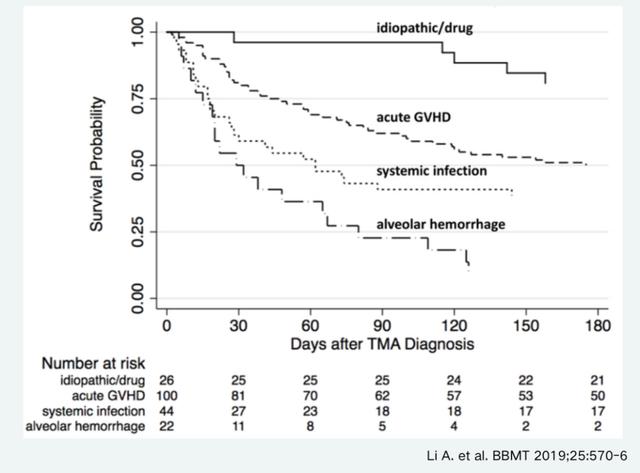
图三展示了TA-TMA的危险因素对预后的影响。药物诱发的TA-TMA是预后最好的,停药后很多人可自行恢复。其次是急性GVHD诱发的TA-TMA,如果GVHD得到有效的控制,这些患者很多也是可以恢复的。如果是严重感染诱发的TA-TMA,预后就比较差。肺泡出血伴发的TA-TMA,预后是最差的。
图三. TA-TMA的危险因素对预后的影响
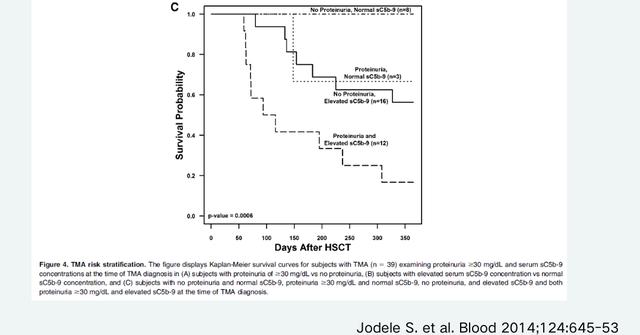
大量蛋白尿(尿蛋白≥30mg/dL),血浆活化补体C5b-9水平升高,是TA-TMA的预后不良因素。如图四所示TA-TMA的预后与上述两个指标密切相关,生存率从高到底依次为:无大量蛋白尿且血浆C5b-9水平正常者>大量蛋白尿或血浆C5b-9水平升高者>大量蛋白尿且血浆C5b-9水平升高者。
图四. 大量蛋白尿与血浆C5b-9水平升高对TA-TMA预后的影响
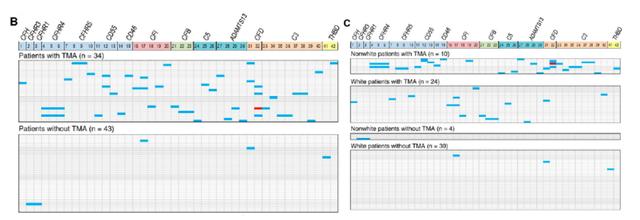
图五左图显示发生TA-TMA者与未发生TA-TMA者相比与补体激活相关基因的变异明显增多。图五右图显示在发生TA-TMA的患者中非白人(主要为黑人)与白人相比与补体激活相关基因的变异明显增多。说明TA-TMA的发生与遗传易感性及种族有关。
图五 补体激活相关基因的变异及种族对TA-TMA的影响
04
TA-TMA的临床表现
TA-TMA累及不同的器官会出现相应的临床表现,肾脏为最常累及的器官,主要表现为肾功能下降(肾小球滤过率下降、蛋白尿、高血压);累及肺可表现为肺动脉高压及低氧血症;累及胃肠道可表现为恶心呕吐、腹泻、腹痛、出血;累及中枢神经系统可出现神志改变、头痛、幻觉、抽搐;此外有些患者临床上GVHD表现不明显,但以多浆膜腔积液为表现,如心包积液、胸水、腹水。
05
TA-TMA的诊断
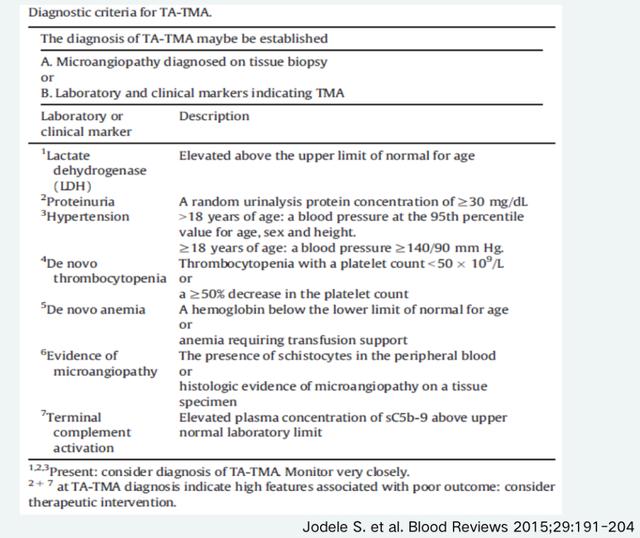
目前的诊断标准包括7条,如图六所示:乳酸脱氢酶(LDH)升高,大量蛋白尿,高血压,血小板减少,贫血,微血管病(外周血破碎红细胞或组织病理证实),补体激活。同时出现大量蛋白尿和血浆激活补体C5b-9升高者为重型TA-TMA,预后差。
图六. TA-TMA诊断标准
TA-TMA的确诊靠病理,比如肾或肠道活检看到广泛的微血栓形成即可明确诊断,但TA-TMA患者常血小板显著降低,一般状况差,许多病例无条件做活检。这时可以查血的破碎红细胞、血浆活化补体C5b-9的水平等协助诊断。
关于TA-TMA的诊断,哪些指标异常会出现得更早一些呢?如图七所示,高血压、LDH升高和蛋白尿会出现的最早,随后才能检出血中破碎红细胞的增加,出现肌酐升高已经是比较后期的表现了,而在儿童肌酐升高更少见,因此,高血压、LDH升高和蛋白尿是诊断TA-TMA较敏感的指标,有利于早诊断。
图七. TA-TMA相关指标异常发生的顺序
06
TA-TMA的治疗
TA-TMA的治疗,通常第一步要减停可疑的药物,比如环孢素、他克莫司、西罗莫司。因为如果是药物引起的,停药后多会自行恢复,这是最简单易行的。如果患者合并有GVHD,在停用上述抗GVHD的药物后,可用骁悉、肾上腺皮质激素、舒莱等药物来替代。
同时要把可能诱发TA-TMA的因素去除、控制,比如说患者有病毒感染、GVHD等,要积极控制病毒感染或GVHD。同时也要重视症状管理,重症TA-TMA患者往往有顽固性高血压,需要两种或者两种以上的降压药物才能控制,控制好高血压可以减少脑出血等严重合并症的风险。高血压的控制,首选ACEI类的药物,既能控制高血压,又能减少尿蛋白的丢失。
重型TA-TMA要尽早使用补体单抗eculizumab,但此药费用昂贵,也可以选择去纤苷治疗。另外,血浆置换对TTP是很有效的,但对TA-TMA疗效并不是很好,有效率不到50%,但血浆置换本身风险较低,也不增加感染的机会,可能会去掉一些有害的物质,所以是可以用于TA-TMA治疗的。有学者提出用CD20单抗治疗TA-TMA,原因是TA-TMA有一部分的发病机制是因为产生了一些针对内皮保护因子的抗体,但CD20单抗可能会增加感染的机会,要权衡利弊,使用时要注意预防及控制感染。
小结:
TA-TMA是微血管内皮损伤所致的多器官疾病,肾是最常受累的器官,但肺、胃肠道和中枢神经系统的病变也不容忽略。当HSCT患者出现LDH急性升高,伴有蛋白尿、高血压及血的破碎红细胞增多时应怀疑TA-TMA,补体系统的调节异常对TA-TMA的严重度起重要作用。当蛋白尿≥30mg/dL且血浆C5b-9水平升高时属高危TA-TMA,预后差,应立即采用补体单抗eculizumab或其它有效治疗,诱因的去除与控制很重要,强调早诊断、早治疗,以提高疗效。
专家介绍
吴彤
高博医学(血液病)北京研究中心北京博仁医院医疗院长,血液二科(移植技术)主任,毕业于北京医科大学医疗系,在美国国立卫生研究院(NIH)心肺血液所做造血干细胞基因治疗方面的博士后研究4年。
具有30余年造血干细胞移植经验,是国际知名的造血干细胞移植专家,擅长造血干细胞移植(HSCT)治疗白血病、MDS、淋巴瘤、再生障碍性贫血、噬血细胞综合征等疾病及移植合并症的防治。
现为中华医学会血液学分会会员、美国血液学会会员、国际血液学会会员、亚太骨髓移植学会(APBMT)会员及学术委员会委员、中国抗癌协会血液肿瘤专业委员会副主任委员(前任)及移植与细胞治疗学组副组长、女医师协会临床肿瘤专业委员会青年委员及血液专业委员会常委、中国医师协会整合医学分会整合血液病专业委员会委员、《中华血液学杂志》编委、《Hematology/Oncology and Stem Cell Therapy》编委、《Blood》杂志中国版编委。
整理丨Lily
审核丨吴彤主任
高博医学论坛
您的血液学术生态圈
为您提供您所关注的血液学最新学术活动讯息、科研前沿进展、临床专家观点、疑难病例分享、各类指南及学习资料等,欢迎各位医生、研究者关注!